|
Станнан
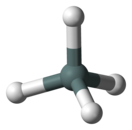
Станна́н (тетрагидри́д о́лова, гидри́д олова(IV), оловя́нистый водоро́д, моностанна́н, станномета́н) — бинарное неорганическое химическое соединение олова и водорода. Химическая формула . Чрезвычайно ядовит. Как и другие высшие гидриды элементов четвёртой группы (силан , герман , плюмбан ), является аналогом метана . Одновалентный радикал называется станнил. Химические свойстваОчень нестоек. Нацело разлагается водой. На воздухе самовоспламеняется:
Не проявляет кислотных или щелочных свойств. При взаимодействии с галогенами с взрывом очень большой мощности все атомы водорода замещаются на галоген:
Станнан термодинамически неустойчив, при нормальных условиях постепенно разлагается с образованием оловянного зеркала:
Самопроизвольный распад связан с тем, что олово — продукт реакции распада — является её катализатором, то есть реакция распада станнометана (и других гидридов олова) является автокаталитической. При температуре выше +160 °C разлагается со взрывом. Примесь небольшого количества газообразного кислорода (~10 %) стабилизирует станнан, и его можно хранить при комнатной температуре. Разложение ускоряется при контакте с резиной, а также с шероховатыми, металлическими или покрытыми жиром поверхностями. Физические свойстваПри нормальных условиях станнан является бесцветным тяжёлым газом (плотность 5,4 г/л). Температура кипения −51,8 °C, температура плавления −146 °C. Энергия связи Sn—H равна 297 кДж/моль, длина связи 170 пм. Теплота образования равна −163 кДж/моль. ПолучениеПолучается по реакции станнидов с кислотами:
При взаимодействии солей олова с активными металлами в кислой среде:
При восстановлении хлорида олова(IV) алюмогидридом лития:
Станнан образуется также при восстановлении солей олова цинком в соляной кислоте. В некоторых из перечисленных реакций образуется также водород, от которого станнан может быть отделён охлаждением до температуры конденсации. Станнан может образовываться при реакции металлического олова с органическими кислотами. С этим связаны тяжёлые отравления консервированными продуктами, долго хранившимися в лужёных банках. ПрименениеПочти не применяется ввиду своих свойств. Добавляется в сварочный состав в сверхнизких количествах. Используется как промежуточное сырье при получении оловосодержащих полимеров и других оловоорганических веществ. Биологическое воздействие Сильнейший яд, сравним по токсичности с арсином (мышьяковистым водородом). См. такжеПримечания
Ссылки
Литература
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||