|
Гипоглицин
Гипоглицин (также Гипоглицин А) — органическое соединение, фитотоксин, непротеиногенная аминокислота, производная L-аланина[1], является высокотоксичным веществом. Контаминант. Нахождение в природе Гипоглицин встречается в незрелых плодах, а также в семенах Аки, или Блигии вкусной (Blighia sapida), где его концентрация в 2-3 раза больше. Плоды этого дерева разрешены к употреблению, только когда они раскроются и будут видны чёрные семена. Содержание в незрелых плодах — свыше 0,1 %, тогда как в спелых снижается до 0,1·10−4 %[2]. В 2017 году было обнаружено, что гипоглицин также содержится в незрелых плодах личи (Litchi chinensis)[3], открытие было сделано в результате массовых отравлений с летальным исходом детей в Индии, которые употребляли незрелые плоды личи. ТоксичностьНа Ямайке среди бедного населения встречается эндемическое заболевание, которое, как уже давно замечено, связано с употреблением в пищу незрелых плодов Аки (Blighia sapida) — Ямайская рвотная болезнь. Это заболевание характеризуется гипогликемией (пониженным содержанием сахара в крови) и нарушением обмена жирных кислот. Токсическое действие плодов Blighia sapida обусловливается содержащимся в них гипоглицином, представляющим собой производное пропионовой кислоты. В процессе метаболизма гипоглицин превращается в вещество, которое в форме соответствующего КоА-эфира является мощным и специфическим ингибитором окисления КоА-эфиров жирных кислот с короткой цепью, главным образом бутироил-КоА. В присутствии этого вещества бутироил-КоА гидролизуется с образованием свободного бутирата, который в избытке накапливается в крови и косвенным путём вызывает гипогликемию[4]. Для людей ЛД50 составляет 40 мг/кг[5]. СинтезВ 1958 году Джон Карбон, Уильям Мартин, и Лео Светт были первыми, кто синтезировал гипоглицин в виде рацемата. Синтез начинается с взаимодействия 2-бромпропена и этилдиазоацетата с образованием циклопропанового производного и последующих реакций гидроалкилирования, взаимодействия с тозилатом, гидридом натрия в растворе диметилформамида и ацетилирования в щелочной среде[6]. 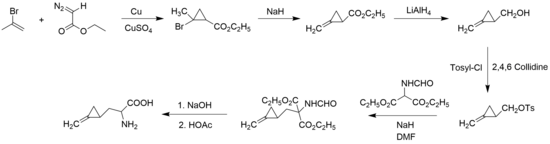 См. такжеПримечания
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
