Álcool benzílico
Alerta sobre risco à saúde
|
|
|
| Nome IUPAC
|
Fenilmetanol, álcool benzílico [1]
|
| Outros nomes
|
Fenilcarbinol
|
| Identificadores
|
| Número CAS
|
100-51-6
|
| SMILES
|
|
| Propriedades
|
| Fórmula molecular
|
C7H8O
|
| Massa molar
|
108.14 g/mol
|
| Densidade
|
1.044 g/cm3
|
| Ponto de fusão
|
-15 °C
|
| Ponto de ebulição
|
205 °C
|
| Riscos associados
|
| MSDS
|
ScienceLab.com
|
| NFPA 704
|
|
| Ponto de fulgor
|
101°C (374 K)
|
| LD50
|
1250 mg/kg (rato, oral)
|
| Compostos relacionados
|
| Outros aniões/ânions
|
Benzilamina
Fluoreto de benzila
Benzil mercaptano
|
| Compostos relacionados
|
Ácido benzoico
Benzaldeído
Tolueno
Cresol
2-Feniletanol
Acetato de benzila
Álcool salicílico (álcool 2-hidroxibenzílico)
|
| Página de dados suplementares
|
| Estrutura e propriedades
|
n, εr, etc.
|
| Dados termodinâmicos
|
Phase behaviour
Solid, liquid, gas
|
| Dados espectrais
|
UV, IV, RMN, EM
|
Exceto onde denotado, os dados referem-se a
materiais sob condições normais de temperatura e pressão
Referências e avisos gerais sobre esta caixa.
Alerta sobre risco à saúde.
|
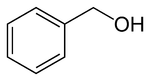
Álcool benzílico é um composto orgânico com a fórmula C6H5CH2OH. O grupo benzila é comumente abreviado "Bn", então temos BnOH, para o álcool benzílico. O álcool benzílico é um líquido incolor com um medianamente agradável odor aromático.
Ocorrência e preparação
É um constituinte natural de uma variedade de óleos essenciais incluindo jasmim, jacinto, e ylang-ylang.[2] Álcool benzílico é também um solvente usual devido a sua polaridade, baixa toxicidade, e baixa pressão de vapor.
Álcool benzílico é parcialmente solúvel em água (4 g/100 ml) e completamente solúvel em álcoois e éter dietílico. É preparado pela hidrólise de cloreto de benzila usando hidróxido de sódio:
- C6H5CH2Cl + NaOH → C6H5CH2OH + NaCl
Ele também pode ser preparado via a reação de Grignard por reagir brometo de fenilmagnésio (C6H5MgBr) com formaldeído, seguido por acidificação. Como muitos álcoois, reage com ácidos carboxílicos para formar ésteres.
Aplicações
Álcool benzílico é usado como um solvente geral para tintas, lacas e revestimentos a base de resinas epóxi.[3] É também um precursor para uma variedade de ésteres, usados em sabões, perfumes, e flavorizantes, assim como na síntese de fármacos. Exibe propriedades bacteriostáticas e antipruriginosas. É usado também em fotografia.
Usos ilustrativos em síntese orgânica
Em síntese orgânica, ésteres benzílicos são grupos protetores populares porque eles podem ser removidos por suave hidrogenólise.[4]
BnOH reage com acrilonitrila resultando em N-benzilacrilamida. Isto é um exemplo de uma reação de Ritter:[5]
- C6H5CH2OH + NCCHCH2 → C6H5CH2N(H)C(O)CHCH2
Usos em nanotecnologia
Álcool benzílico tem sido usado como um solvente dielétrico para a reconfiguração dieletroforética de nanofios.[6]
Ligações externas
Referências
- ↑ Pubchem. «benzyl alcohol». pubchem.ncbi.nlm.nih.gov (em inglês). Consultado em 27 de setembro de 2017
- ↑ Merck Index, 11th Edition, 1138.
- ↑ «Benzyl alcohol at chemicalland21.com». Consultado em 29 de Março de 2008. Arquivado do original em 21 de Abril de 2009
- ↑ Furuta, K.; Gao, Q.-Z.; Yamamoto, H. (1998). «Chiral (Acyloxy)borane Complex-Catalyzed Asymmetric Diels-Alder Reaction: (1R)-1,3,4-Trimethyl-3-Cyclohexene-1-Carboxaldehyde». Org. Synth. ; Coll. Vol., 9
- ↑ Parris, C. L. (1973). «N-benzylacrylamide». Org. Synth. ; Coll. Vol., 5
- ↑ Alexander Wissner-Gross (19 de outubro de 2006). «Nanowires get reconfigured». Nanotechweb.org. Consultado em 29 de Março de 2008. Arquivado do original em 22 de Maio de 2007


