|
Hydroksyloamina
Hydroksyloamina
|
|
|
|
|
| Ogólne informacje
|
| Wzór sumaryczny
|
H3NO
|
| Inne wzory
|
NH2OH
|
| Masa molowa
|
33,03 g/mol
|
| Wygląd
|
białe płatki lub igły[2]
|
| Identyfikacja
|
| Numer CAS
|
7803-49-8
|
| PubChem
|
787
|
|
|
| InChI
|
InChI=1S/H3NO/c1-2/h2H,1H2
|
| InChIKey
|
AVXURJPOCDRRFD-UHFFFAOYSA-N
|
|
|
|
|
|
| Niebezpieczeństwa
|
| Karta charakterystyki: dane zewnętrzne firmy Sigma-Aldrich [dostęp 2017-01-04]
|
|
|
Globalnie zharmonizowany system
klasyfikacji i oznakowania chemikaliów
|
Na podstawie Rozporządzenia CLP, zał. VI[3]
hydroksyloamina >55% (roztwór wodny)
|
|
|
|
|
| Zwroty H
|
H200, H290, H302, H312, H315, H318, H317, H335, H351, H373, H400
|
| Zwroty P
|
brak wiarygodnych danych
|
|
|
Na podstawie Rozporządzenia CLP, zał. VI[3]
hydroksyloamina ≤55% (roztwór wodny)
|
|
|
|
|
| Zwroty H
|
H290, H302, H312, H315, H318, H317, H335, H351, H373, H400
|
| Zwroty P
|
P261, P273, P280, P305+P351+P338[4]
|
|
|
| NFPA 704
|
Na podstawie
podanego źródła[5]
hydroksylamina 50% (roztwór wodny)
|
|
|
|
|
| Numer RTECS
|
NC2975000
|
| Dawka śmiertelna
|
LD50 29 mg/kg (szczur, podskórnie)
|
|
| Podobne związki
|
| Podobne związki
|
hydrazyna, nadtlenek wodoru, chloroamina
|
Jeżeli nie podano inaczej, dane dotyczą
stanu standardowego (25 °C, 1000 hPa)
|
|
|
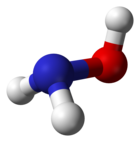
Hydroksyloamina – nieorganiczny związek chemiczny, pochodna amoniaku, w której jeden atom wodoru został zastąpiony grupą hydroksylową. Najprostsza hydroksyamina.
Jest to bezbarwne higroskopijne, krystaliczne ciało stałe o temperaturze topnienia wynoszącej 33,1 °C. Jest silnie trująca, podczas ogrzewania rozkłada się z wydzieleniem ciepła.
Dobrze rozpuszcza się w wodzie i metanolu. Dobra substancja redukująca, czasem może jednak być utleniaczem. Słabo zasadowa, tworzy sole, z których najważniejsze to chlorowodorek hydroksyloaminy i siarczan hydroksyloaminy. Sole te są trwalsze niż wolna hydroksyloamina, ale również trujące.
Otrzymywana przez redukcję kwasu azotowego lub tlenków azotu (z wyjątkiem N
2O) w roztworze kwaśnym albo przez działanie zasadą na chlorowodorek lub siarczan hydroksyloaminy i oddestylowanie zmniejszonym ciśnieniem wydzielającej się hydroksyloaminy.
Stosowana jako środek redukujący i odczynnik w syntezie organicznej, np. do otrzymywania oksymów[6]:
- R
2C=O + NH
2OH → R
2C=NOH + H
2O
Działanie hydroksyloaminy na organizm człowieka jest bardzo negatywne. Ma właściwości mutagenne. Reaguje z cytozyną w DNA, zamieniając ją na związek zbliżony do uracylu, działa też na enzymy komórkowe. W wyniku jej działania powstają często groźne mutacje punktowe[7][niewiarygodne źródło?].
Przypisy
- ↑ a b c Neil G.N.G. Connelly Neil G.N.G. i inni, Nomenclature of Inorganic Chemistry. IUPAC Recommendations 2005 (Red Book), International Union of Pure and Applied Chemistry, RSC Publishing, 2005, s. 309, ISBN 978-0-85404-438-2 (ang.).
- ↑ a b c d e f g h CRC Handbook of Chemistry and Physics, William M.W.M. Haynes (red.), wyd. 97, Boca Raton: CRC Press, 2016, s. 4-65, 5-87, 9-63, ISBN 978-1-4987-5429-3 (ang.).
- ↑ a b hydroksyloamina ...%, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów [dostęp 2017-01-04] (ang.).
- ↑ Hydroksyloamina, roztwór (nr 467804) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Polski. [dostęp 2017-01-04]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Hydroksyloamina (nr 467804) (ang.) – karta charakterystyki produktu Sigma-Aldrich (Merck) na obszar Stanów Zjednoczonych. [dostęp 2017-01-04]. (przeczytaj, jeśli nie wyświetla się prawidłowa wersja karty charakterystyki)
- ↑ Robert T. Morrison, Robert N. Boyd: Chemia organiczna. T. 1. Warszawa: PWN, 1985, s. 732. ISBN 83-01-04166-8.
- ↑ Tablice biologiczne, WitoldW. Mizerski (red.) i inni, Warszawa: Adamantan, 2013, s. 302, ISBN 978-83-7350-243-7, OCLC 891265110 .
Bibliografia
|
|