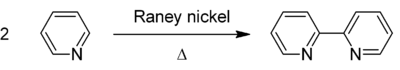2,2'-bipyridine
Structuurformule en molecuulmodel
Algemeen
Molecuulformule
C10 H8 N2
IUPAC-naam
2,2'-bipyridine
Andere namen
2,2'-dipyridyl, α,α'-bipyridyl, 2-(2-pyridyl)pyridine, bipyridyl, dipyridyl, bipy, bpy, dipy
Molmassa
156,18 g /mol
SMILES
C1(C2=CC=CC=N2)=NC=CC=C1
CAS-nummer
366-18-7
EG-nummer
206-674-4
Wikidata
Q209143
Beschrijving
Kleurloze tot witte kristallen
Waarschuwingen en veiligheidsmaatregelen
Gevaar
H-zinnen
H301 - H315 - H319 - H335
EUH-zinnen geen
P-zinnen
P261 - P301+P310 - P305+P351+P338
Opslag
Gescheiden van sterk oxiderende stoffen.
Fysische eigenschappen
Aggregatietoestand
vast
Kleur
kleurloos-wit
Smeltpunt
70-73 °C
Kookpunt
273 °C
Oplosbaarheid in water
64 g/L
Goed oplosbaar in
water
Geometrie en kristalstructuur
Dipoolmoment
0 D
Tenzij anders vermeld zijn standaardomstandigheden gebruikt (298,15 K of 25 °C , 1 bar ).
2,2'-bipyridine is een organische verbinding met als brutoformule C10 H8 N2 . Het bestaat uit kleurloze tot witte kristallen , die oplosbaar zijn in water . Het is een van de isomeren van bipyridine .
Synthese
2,2'-bipyridine wordt gesynthetiseerd door pyridine te dehydrogeneren , met raneynikkel als katalysator :[ 1]
Synthese van 2,2'-bipyridine
Daarnaast zijn uitgaande van pyridine synthesen bij 330°C met ijzer(III)chloride als katalysator[ 2] 2-broompyridine via een Ullmann-reactie waarbij metallisch koper als katalysator optreedt.[ 3]
Toepassing
2,2'-bipyridine wordt gebruikt voor de bereiding van het herbicide diquat . De reactie met 1,2-dibroomethaan levert diquatdibromide .[ 4]
Het wordt ook als bidentate ligand gebruikt bij de productie van weekmakers .
Toxicologie en veiligheid
De stof vormt bij verbranding giftige gassen, waaronder stikstofoxiden . Ze reageert met oxiderende stoffen .
Externe links
Bronnen, noten en/of referenties
↑ W. H. F. Sasse: 2,2′-Bipyridine , in: Org. Synth. Coll. Vol. 1973 , 5 , S. 102.
↑ F. Hein, H. Schwedler: Zur α,α-Dipyridyl-Synthese aus Pyridin und Eisen(III)-chlorid, sowie über einige Dipyridyl-Komplexsalze , in: Chem. Ber. 1935 , 68 , pp. 681–684; DOI :10.1002/cber.19350680425
↑ F. H. Burstall: Researches on the polypyridyls , in: J. Chem. Soc. 1938 , pp. 1662–1671; DOI :10.1039/JR9380001662 .
↑ Thomas A. Unger, "Pesticide Synthesis Handbook" (1996), blz. 504