|
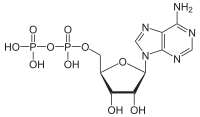
ポリリン酸ポリリン酸(ポリりんさん、英: polyphosphoric acid)は、酸素原子を共有して結合した四面体 PO4(リン酸)構造単位からなるポリマーのオキソ酸である。また、その塩やエステルについてもこの記事で説明する。2つの角が共有されたポリリン酸イオンは直鎖構造または環状構造をとることがある。生物学ではポリリン酸エステルであるアデノシン一リン酸、アデノシン二リン酸、およびアデノシン三リン酸(ATP)がエネルギーの移動に関与する。 さまざまなポリリン酸塩が一般的に1 - 5 mg/Lの濃度で都市用水でのミネラル隔離に利用される[1]。 構造と化学式
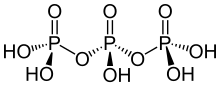
三リン酸の構造を用いてポリリン酸の構造を決める原則を説明する。三リン酸は酸素原子を共有して結合した3つの四面体の PO4 単位からなる。構造的に外側の四面体は中心の四面体と1つの頂点を共有しており、中央の四面体は外側の四面体と2つの頂点を共有している。相当するリン酸は酸性プロトンを失って酸と結合する。環状トリマーの場合には、それぞれの四面体は隣の四面体と2つの頂点を共有している。 層状ケイ酸塩鉱物のように3つの角を共有することも可能であるが、そのような構造は極端な環境下でのみ見られる。3つの角を共有する構造は3次元構造を持つ五酸化二リン (P4O10) でも見られる。 化学的には、重合反応は縮合反応として見られる。その過程は2つのリン酸単位が反応して始まる。
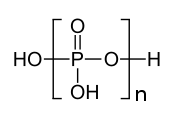
この反応は可逆的であるため平衡反応であることが示されており、逆反応は水分子で分解されるため 加水分解反応と呼ばれる。縮合反応は次のように段階的に進行する。各段階で1つの PO3 単位が鎖に加えられ、上で示したポリリン酸の図の n が1つ増える。P4O10 は縮合反応の最終産物として見られ、それぞれの四面体の3つの角は他のものと共有されている。反対に、五酸化二リンに少量の水を加えるとポリマーの複雑な混合物が得られる。 酸塩基および錯形成ポリリン酸イオンは弱塩基である。酸素原子の孤立電子対は典型的なルイス酸-ルイス塩基相互作用でプロトンまたは金属イオンに供与されることがある。これは生物学的に非常に重要である。例えば、ATP はpH 7の水溶液では25 %がプロトン化されている[2]。
それより低い pH ではさらにプロトン化が起こる。 ATP は金属イオンとキレート錯体を形成する。その平衡の安定度定数
は特に大きい[3]。マグネシウムとの錯形成は、末端のリン酸基と他の部分との結合を弱めるため、ATP の加水分解過程で決定的な因子である[2][4]。 「高エネルギー」リン酸結合→詳細は「高エネルギーリン酸結合」を参照
ATP の加水分解で放出されるエネルギーは、
で示され、Pi は無機リン酸を示し、生物学的な pH ではプロトン化されている。その時の ΔG —36.8 kJ mol−1 は生物学的な基準では大きい。 高分子無機ポリリン酸塩高分子無機ポリリン酸塩(こうぶんしむきポリリンさんえん、英: high-polymeric inorganic polyphosphates)は1890年に生物から L. Liberman によって発見された。その化合物は直鎖のポリマーでエネルギーに富むリン酸無水物結合によって結合した数個から数百個のオルトリン酸残基を含んでいた。 以前は、この化合物は「分子化石」またはただのリン酸塩であり、極限環境下で微生物が生き残るためのエネルギー源を供給しているに過ぎないと考えられていた。この化合物は現在、調節の役割を持ち、すべての界の生物で見られ、代謝の補正および遺伝子と酵素のレベルでの調節に関与している。ポリリン酸塩は、対数増殖期のバクテリアに特徴的な遺伝子プログラムを、定常状態下での細胞の生き残りに関するプログラムに変える機構に直接関わっている。ポリリン酸塩はバクテリアにおいて次に示すような多くの調節機構に関与している。
ヒトでは、ポリリン酸塩は凝血に重要な役割を持つことが知られている。血小板によって産生され、放出されたポリリン酸塩は、血餅形成に不可欠な第XII因子を活性化する。さらに、血小板由来のポリリン酸塩は、フィブリン形成を開始する血液凝固第XII因子(ハーゲマン因子)や前炎症性メディエータの生成、および血管や血栓症からの滲出に寄与するブラジキニンを活性化する[5][6]。 脚注
関連項目外部リンク
|