|
サキシトキシン
サキシトキシン(英: Saxitoxin、STX)は、主にアレクサンドリウム属(Alexandrium catenella など)の赤潮を形成する有毒渦鞭毛藻がつくる麻痺性毒物の一種。その藻類を食べることで、通常は毒を持たない貝類などが毒化することがある。また、水の華を形成するシアノバクテリア (Anabaena circinalis) や淡水性ラン藻 (Aphanizomenon flos-aquae) などが生産するシアノトキシンの一種である[1][2]。 サキシトキシンは1962年に北米産の二枚貝の学名にちなみ命名され[3]、1975年にSchantzら[4]、Rapoportら[5]によって、X線結晶構造解析により構造決定された。サキシトキシンには約30種の同族体が存在する。 主な保有生物テトロドトキシンと共にフグ毒の成分のひとつ。フグのほか麻痺性貝毒の代表的な成分で主に二枚貝のムラサキイガイ、マガキ、アサリ、ホタテガイなどの中腸腺に蓄積される事がある。また、房総半島以南の磯周りに普通に分布するオウギガニ科(スベスベマンジュウガニ)のカニは筋肉に蓄積することがある。パナマ産のヤドクガエルの一種 (Atelopus zeteki) も保有することが報告されている[6]。 毒性テトロドトキシンと同様に神経などのNa+チャネルを阻害し、舌や唇などの麻痺や[8]、重度の場合には呼吸困難を引き起こし、最終的には呼吸麻痺で死に至る。有効な治療法は確立されていない。 生合成サキシトキシンの生合成経路は複雑だが、その合成能力は海産の渦鞭毛藻、淡水産の藍藻という2つのドメインの生物に跨って存在している。かつて渦鞭毛藻は藍藻との相利共生によってサキシトキシンを獲得していると考えられていたが、渦鞭毛藻自体もサキシトキシンの合成に必要な遺伝子を有していることが示唆されている[9]。 サキシトキシンの生合成経路は細菌による非テルペン系アルカロイドの合成経路として最初に知られたものであるが、正確な合成機構は未だ理論モデルの段階に留まっている。基質が酵素に結合する正確な機構は未だ不明であり、関与する遺伝子も最近になって同定が始められたばかりである[9][10]。以下は、藍藻においてSTX遺伝子クラスター (sxt) の関与を想定した反応モデルである[10]。 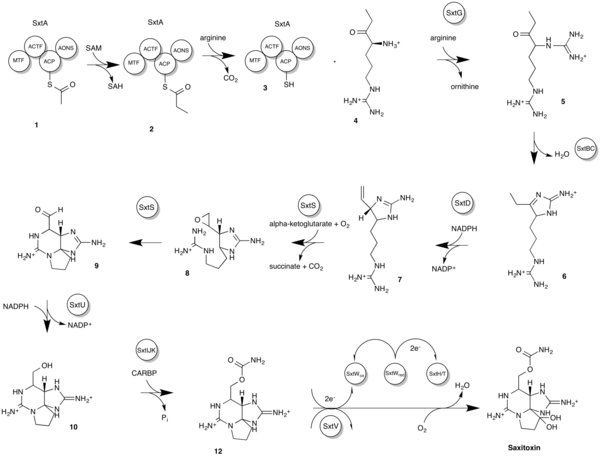
関連法規化学兵器の禁止及び特定物質の規制等に関する法律で特定物質に指定されており製造、使用、所持などが厳しく規制されている。 脚注
関連項目外部リンク
|
||||||||||||||||||||||||
