|
Cycle du dioxyde de siliciumLe cycle du dioxyde de silicium est le cycle biogéochimique dans lequel le dioxyde de silicium SiO2 (ou silice) est transféré entre les différents systèmes terrestres. Le silicium est un élément bioessentiel et c'est aussi l'un des éléments les plus abondants sur Terre[1],[2]. Le cycle du dioxyde de silicium a un chevauchement significatif avec le cycle du carbone (cycle carbonate-silicate) et joue un rôle important dans l'enfermement du carbone par le biais de l'altération continentale, de l'exportation biogénique et de l'enfouissement sous forme de limons à l'échelle des temps géologiques[3]. Cycle de la silice terrestreLa silice est un nutriment important utilisé par les plantes, les arbres et les graminées dans la biosphère terrestre. Le silicate est transporté par les rivières et peut se déposer dans les sols sous la forme de divers polymorphes siliceux. Les plantes peuvent facilement absorber le silicate sous forme de H4 SiO4 pour la formation de phytolithes. Les phytolithes sont de minuscules structures rigides trouvées dans les cellules végétales qui contribuent à l'intégrité structurelle de la plante[1]. Ils servent également à protéger les plantes de la consommation par les herbivores qui ne peuvent consommer et digérer efficacement les plantes riches en silice. On estime que la libération de silice due à la dégradation ou à la dissolution des phytolithes se produit à un taux double de celui de l'altération globale des minéraux silicatés[2]. Compte tenu du cycle biogéochimique au sein des écosystèmes, l'importation et l'exportation de silice vers et depuis les écosystèmes terrestres sont faibles. SourcesLes minéraux silicatés sont abondants dans les formations rocheuses de toute la planète, comprenant environ 90% de la croûte terrestre[3]. La principale source de silicate dans la biosphère terrestre est l' altération. Un exemple de réaction chimique pour cette altération est:
La wollastonite (CaSiO 3 ) et l' enstatite (MgSiO 3 ) sont des exemples de minéraux à base de silicate[4]. Le processus d'altération est important pour la séquestration du carbone à des échelles de temps géologiques[2]. Le processus et le taux d'altération sont variables en fonction des Les précipitations, les ruissellement, la végétation, la lithologie et la topographie sont les principales variables pour le processus et le taux d'altération. PuitsL'exportation vers l'océan par les rivières de la silice stockée dans la matière végétale est le principal puits du cycle de la silice terrestre. Le taux de ce transport est d'environ 6 Tmol Si an -1[5],[2]. C'est également la plus grande source du cycle de la silice marine. Un puits mineur pour la silice terrestre est le silicate qui est déposé dans les sédiments terrestres et finalement exporté vers la croûte terrestre. Cycle de la silice marine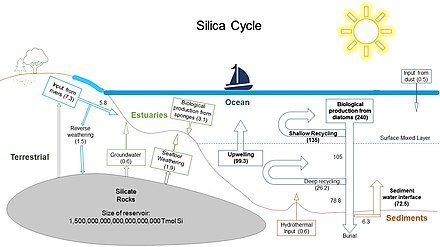 Les organismes siliceux de l'océan, tels que les diatomées et les radiolaires, sont le principal puits d'acide silicique dissous dans la silice opale[10]. Une fois dans l'océan, les molécules de Si dissoutes sont recyclées biologiquement environ 25 fois avant l'exportation et le dépôt permanent dans les sédiments marins du fond marin[2]. Ce recyclage rapide dépend de la dissolution de la silice dans la matière organique dans la colonne d'eau, suivie d'une absorption biologique dans la zone photique. Le temps de séjour estimé du réservoir biologique de silice est d'environ 400 ans. La silice opale est principalement sous-saturée dans les océans du monde. Cette sous-saturation favorise une dissolution rapide du fait d'un recyclage constant et de longs temps de séjour. Le temps de renouvellement estimé du Si est de 1,5 x 10 4 ans[5]. Les entrées et sorties nettes totales de silice dans l'océan sont respectivement de 9,4 ± 4,7 Tmol Si an −1 et 9,9 ± 7,3 Tmol Si an −1. La production de silice biogénique dans la zone photique est estimée à 240 ± 40 Tmol Si an -1[5]. La dissolution en surface élimine environ 135 Tmol de Si par an -1, tandis que le Si restant est exporté vers l'océan profond dans des particules qui coulent[2]. Dans l'océan profond, un autre 26,2 Tmol Si Year −1 est dissous avant d'être déposé dans les sédiments sous forme de pluie d'opale. Plus de 90% de la silice est ici dissoute, recyclée et éventuellement remontée pour être réutilisée dans la zone euphotique. SourcesLes principales sources de silice marine comprennent les rivières, le flux des eaux souterraines, les apports d'altération du fond marin, les évents hydrothermaux et les dépôts atmosphériques ( flux éolien )[4]. Les rivières sont de loin la plus grande source de silice du milieu marin, représentant jusqu'à 90% de toute la silice livrée à l'océan[5],[13]. Une source de silice pour le cycle biologique de la silice marine est la silice qui a été recyclée par remontée des eaux profondes des océans et des fonds marins. PuitsLe dépôt des fonds marins est le plus grand puits à long terme du cycle de la silice marine (6,3 ± 3,6 Tmol Si an −1 ), et est à peu près équilibré par les sources de silice dans l'océan[4]. La silice déposée dans l'océan profond se présente principalement sous forme de limon siliceux, qui est finalement subduit sous la croûte et métamorphosé dans le manteau supérieur[14]. Sous le manteau, les minéraux silicatés se forment dans les suintements et sont finalement remontés à la surface. En surface, la silice peut à nouveau entrer dans le cycle par vieillissement, cela peut prendre des dizaines de millions d'années. Le seul autre grand puits de silice dans l'océan est l'enfouissement le long des marges continentales (3,6 ± 3,7 Tmol Si an −1 ), principalement sous forme d' éponges siliceuses. En raison du degré élevé d'incertitude dans les estimations des sources et des puits, il est difficile de conclure si le cycle de la silice marine est en équilibre. Le temps de séjour de la silice dans les océans est estimé à environ 10 000 ans. La silice peut également être retirée du cycle en devenant chert et en étant enterrée en permanence. Influences anthropiquesL'essor de l'agriculture au cours des 400 dernières années a augmenté l'exposition aux roches et aux sols, ce qui a entraîné une augmentation des taux d'altération des silicates. À son tour, le lessivage des stocks de silice amorphe des sols a également augmenté, entraînant des concentrations plus élevées de silice dissoute dans les rivières[4]. À l'inverse, l'augmentation des barrages a conduit à une réduction de l'approvisionnement en silice dans l'océan en raison de l'absorption par les diatomées d'eau douce derrière les barrages. La prédominance du phytoplancton non siliceux en raison de la charge anthropique d'azote et de phosphore et de la dissolution accrue de la silice dans les eaux plus chaudes a le potentiel de limiter l'exportation de sédiments océaniques de silicium à l'avenir. Rôle dans la régulation climatiqueLe cycle de la silice joue un rôle important dans la régulation climatique mondiale à long terme. Le cycle global de la silice a également des effets importants sur le cycle global du carbone à travers le cycle carbonate-silicate[15]. Le processus d'altération des minéraux silicatés transfère le CO2 atmosphérique au cycle hydrologique par la réaction chimique présentée ci-dessus[3]. Sur les échelles de temps géologiques, les taux d'altération changent en raison de l'activité tectonique. Pendant une période de taux de soulèvement élevé, l'altération des silicates augmente, ce qui entraîne des taux élevés d'absorption de CO2, compensant l'augmentation des émissions de CO2 volcanique associées à l'activité géologique. Cet équilibre entre les intempéries et les volcans fait partie de ce qui contrôle l' effet de serre et le pH des océans sur des échelles de temps géologiques. Notes et références
|
