|
Ácido fluoroantimónico
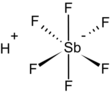
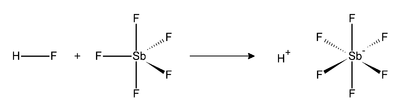
El ácido fluoroantimónico (HSbF6) es una mezcla de fluoruro de hidrógeno y pentafluoruro de antimonio en diversas proporciones.[2] La proporción 1:1 conduce al superácido más fuerte conocido, el cual se ha demostrado que protona incluso a los hidrocarburos para producir carbocationes e H2. El ácido fluoroantimónico es el más corrosivo de los llamados super ácidos.[3] La reacción de fluoruro de hidrógeno (HF) y SbF5 es exotérmica. HF libera el catión (H+), y su base conjugada (F−) es secuestrada por una o más moléculas de SbF5 para producir SbF6− octaédrico. Este anión se clasifica como no coordinante, porque es tanto un nucleófilo débil y una base muy débil. El catión H+ permanece efectivamente «desnudo», lo que trae como consecuencia la extrema acidez del sistema. El ácido fluoroantimónico es 2×1019 veces más fuerte que el ácido sulfúrico. La reacción del fluoruro de hidrógeno y pentafluoruro de antimonio procede como sigue: EstructuraSe han cristalizado dos productos relacionados con las mezclas HF-SbF5, y ambos han sido analizados por cristalografía de rayos-X de un solo cristal. Estas sales tienen las fórmulas [H2F+][Sb2F11−] y [H3F2+][Sb2F11−]. En ambas sales, el anión es Sb2F11−.[4] Como se mencionó anteriormente, SbF6− está clasificado como una base débil; el monoanión de mayor tamaño Sb2F11− sería más débil aún. Comparación con otros ácidosLos siguientes valores están basados en la función de acidez de Hammett. La acidez se indica con valores negativos de H0.
AplicacionesEste ácido extraordinariamente fuerte protona casi todos los compuestos orgánicos. En 1967, Bickel y Hogeveen mostraron que la mezcla HF-SbF5 eliminará H2 del metilpropano y metano del neopentano:[5][6]
SeguridadHF-SbF5 se descompone por acción del agua de forma rápida y explosiva. Reacciona con prácticamente todos los disolventes conocidos. Algunos disolventes que se ha probado que son compatibles con HF-SbF5 son el clorofluoruro de sulfurilo y el óxido de azufre (IV). También se han usado clorofluorocarbonos como disolventes. Los contenedores para HF-SbF5 están hechos de PTFE. (recubrimiento de cohetes, aviones, etc.) Referencias
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||