|
Equilibrio térmico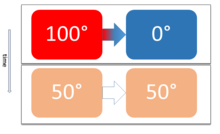 El equilibrio térmico es aquel estado en el cual se igualan las temperaturas de dos cuerpos, las cuales, en sus condiciones iniciales presentaban diferentes valores; una vez que las temperaturas se han equiparado, se suspende la transferencia de calor entre ambos cuerpos, alcanzándose con ello el mencionado equilibrio térmico del sistema termodinámico. Toda sustancia por encima de los 0 kelvin (−273.15 °C) emite calor. Si dos sustancias en contacto se encuentran a diferente temperatura, una de ellas emitirá más calor y calentará a la más fría. El equilibrio térmico se alcanza cuando ambas emiten, y reciben la misma cantidad de calor, lo que iguala su temperatura. Estrictamente sería la misma cantidad de calor por gramo, ya que una mayor cantidad de sustancia emite más calor a la misma temperatura. Definición termodinámica del equilibrio térmicoPara poder dar una definición más precisa del concepto de equilibrio térmico desde un punto de vista termodinámico es necesario definir algunos conceptos. Dos sistemas que están en contacto mecánico directo o separados mediante una superficie que permite la transferencia de calor lo que se conoce como superficie diatérmica, se dice que están en contacto térmico. Consideremos entonces dos sistemas en contacto térmico, dispuestos de tal forma que no puedan mezclarse o reaccionar químicamente. Consideremos además que estos sistemas están colocados en el interior de un recinto donde no es posible que intercambien calor con el exterior ni existan acciones desde el exterior capaces de ejercer trabajo sobre ellos. La experiencia indica que al cabo de un tiempo estos sistemas alcanzan un estado de equilibrio termodinámico que se denominará estado de equilibrio térmico recíproco o simplemente de equilibrio térmico. A partir de ese momento cesaran los cambios que pueden detectarse macroscópicamente y no obstante que la actividad continúa, de algún modo el estado macroscópico ha llegado al equilibrio y se caracteriza porque ambos sistemas tienen la misma temperatura. Interpretación microscópica del equilibrio térmicoLa termodinámica proporciona una descripción macroscópica de los sistemas que estudia, sin hacer hipótesis acerca de la estructura microscópica de los mismos. Sin embargo, existen otras disciplinas, como la física estadística, que estudian los mismos fenómenos de la termodinámica, pero desde un enfoque microscópico. En particular, el concepto de equilibrio térmico está ligado al concepto de temperatura al decir que dos sistemas en equilibrio térmico tienen la misma temperatura. Desde un punto de vista microscópico, la temperatura está asociada a la energía cinética promedio que tienen las partículas que constituyen el sistema, a saber, átomos, moléculas y/o la estructura electrónica de la sustancia que constituye el sistema. Macroscópicamente, esta energía cinética promedio de las partículas de un sistema es lo que en la termodinámica se llama energía interna, que es una energía que depende casi exclusivamente de la temperatura del sistema. A mayor energía cinética promedio de las partículas que constituyen un sistema, mayor energía interna y, en general, mayor temperatura del sistema. La situación de dos sistemas en contacto térmico se interpreta microscópicamente como que las partículas de la superficie de interfase de ambos sistemas son capaces de interactuar entre sí. Básicamente se puede ver que, microscópicamente, las partículas del sistema de mayor temperatura (que tienen mayor energía cinética) van a transferir parte de su energía a las partículas del otro sistema. Se encuentra que esta interacción entre los dos sistemas da lugar a que las partículas de los dos sistemas alcancen la misma energía cinética promedio y, por lo tanto, la misma temperatura. Es decir, desde un punto de vista microscópico, se entiende como equilibrio térmico entre dos sistemas que las partículas de los dos sistemas tengan la misma energía cinética promedio. Desde un punto de vista macroscópico, se dice que los sistemas han alcanzado un estado de equilibrio, cuando bajo las condiciones indicadas en la sección definición termodinámica del equilibrio térmico, se igualan sus temperaturas. En cambio, desde un punto de vista microscópico, el estado de equilibrio se refiere al promedio, ya que los dos sistemas continúan intercambiando energía incluso una vez alcanzado el equilibrio térmico. La energía cinética individual de una partícula no es estacionaria y son, por tanto, diferentes las energías de cada partícula en cada momento. Es el promedio de la distribución de energías de todas las partículas del sistema lo que no cambia en el tiempo. De igual manera que para el caso macroscópico, se puede extender el concepto de equilibrio térmico para un sistema único, en el que en esa situación de equilibrio, las partículas de dos partes cualesquiera del sistema tienen la misma energía cinética promedio. Principio cero de termodinámicaEl concepto de equilibrio térmico es la base del denominado «principio cero de la termodinámica». Este principio proposición fue proferido por R. H. Fowler en 1931 y se enuncia del siguiente modo:
El hecho de haberse enunciado cuando ya existían el primer y segundo principio (pero enunciarse como fundamento indispensable para ambos), fue lo que determinó que se adoptase como nombre principio cero. Aplicación del concepto de equilibrio térmico: termometría Para saber la temperatura de una sustancia o cuerpo, se utiliza un dispositivo que permite determinar su propia temperatura. Tal dispositivo se denomina termómetro. Para determinar la temperatura de un cuerpo, se pone un termómetro en contacto térmico con él hasta que ambos alcanzan el equilibrio térmico. Sabemos que en el equilibrio térmico tanto el cuerpo como el termómetro se encuentran a la misma temperatura. Por ende, la temperatura que indique el termómetro será también la temperatura del cuerpo en cuestión. Se recalca que, lo que un termómetro indica es su propia temperatura, por esto es importante conocer el concepto de equilibrio térmico. Véase tambiénBibliografía
|