|
Digoxigenina |
|---|
 | | General |
|---|
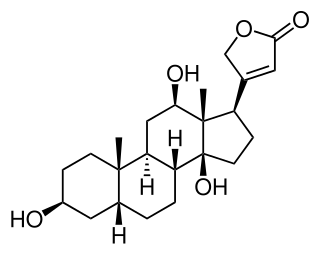
| Fórmula estructural |
 |
|---|
| Fórmula molecular |
? |
|---|
| Identificadores |
|---|
| Número CAS |
1672-46-4[1] |
|---|
| ChEBI |
42098 |
|---|
| ChEMBL |
1153 |
|---|
| ChemSpider |
14728 |
|---|
| DrugBank |
DB03671 |
|---|
| PubChem |
15478 |
|---|
| UNII |
NQ1SX9LNAU |
|---|
O=C/1OCC(=C\1)\[C@@H]2[C@@]4([C@](O)(CC2)[C@@H]5CC[C@@H]3C[C@@H](O)CC[C@]3(C)[C@H]5C[C@H]4O)C
|
InChI= 1S/C23H34O5/c1-21-7-5-15(24)10-14(21)3-4-17-18(21)11-19(25)22(2)16(6-8-23(17,22)27)13-9-20(26)28-12-13/h9,14-19,24-25,27H,3-8,10-12H2,1-2H3/t14-,15+,16-,17-,18+,19-,21+,22+,23+/m1/s1Key: SHIBSTMRCDJXLN-KCZCNTNESA-N | | Propiedades físicas |
|---|
| Masa molar |
390,51 g/mol |
|---|
Valores en el SI y en condiciones estándar
(25 ℃ y 1 atm), salvo que se indique lo contrario. | |
Digoxigenina (DIG), con fórmula química C23H34O5, es un esteroide que se encuentra exclusivamente en las flores y las hojas de las plantas Digitalis purpurea, Digitalis orientalis y Digitalis lanata, donde se une a los azúcares, para formar los glucósidos (por ejemplo lanatoside C).[2]
El uso en la biotecnología
Digoxigenina es un hapteno, una molécula pequeña con alta antigenicidad, que se utiliza en muchas aplicaciones de biología molecular de manera similar a otros haptenos populares, tales como DNP (dinitrofenol), biotina, y fluoresceína. Típicamente, la digoxigenina se introduce químicamente (conjugación) en biomoléculas (proteínas, ácidos nucleicos) para ser detectados en ensayos adicionales. Anti-digoxigenina anticuerpo con altas afinidades y especificidad, se utiliza en una variedad de inmuno-ensayos biológicos (por ejemplo, ELISA). Los anticuerpos están marcados con colorantes, enzimas o fluorescencia, directamente o en segundo lugar, para la visualización y detección.
Digoxigenina es por lo tanto para todo uso inmuno-etiqueta, y, en particular, un estándar de marcador inmunohistoquímica para la hibridación in situ.[3][4] En este caso se conjuga con una sola especie de ARN de nucleótidos trifosfato (típicamente de uridina), que es a continuación, incorporado en ARN (una " ribosonda "), ya que es sintetizada por la maquinaria celular.
Permite realizar:
- sensibilidad no radiactiva en sondas de hibridación in situ para detectar ácidos nucleicos en plantas, capaces de detectar 1 g de ADN plásmido.[5]
- conjugar péptido-DIG, es decir, ensayo de bradicinina por inmunoensayos de quimioluminiscencia muy sensibles.[6]
- trazadores fluorescentes y DIG marcadores para inmunoensayos competitivos, es decir, para detectar digoxina, un medicamento utilizado para curar la arritmia cardiaca, hasta 0.2 ng mL−1.[7]
- Digoxigenina puede conjugarse con azúcares para estudiar eventos de glicosilación,[8] incluso en los sistemas biológicos.
Referencias
- ↑ Número CAS
- ↑ Polya, G. (2003). Biochemical Targets of Plant Bioactive Compounds. New York: CRC Press. ISBN 978-0415308298.
- ↑ Eisel, D.; Grünewald-Janho, S.; Krushen, B., ed. (2002). DIG Application Manual for Nonradioactive in situ Hybridization (3rd edición). Penzberg: Roche Diagnostics.
- ↑ Hauptmann, G.; Gerster, T. (1994). «Two-color whole-mount in situ hybridization to vertebrate and Drosophila embryos». Trends in Genetics 10 (8): 266. PMID 7940754. doi:10.1016/0168-9525(90)90008-T.
- ↑ Hart, S. M.; Basu, C. (2009). «Optimization of a Digoxigenin-Based Immunoassay System for Gene Detection in Arabidopsis thaliana» (pdf). Journal of Biomolecular Techniques 20 (2): 96-100. PMC 2685603. PMID 19503620.
- ↑ Décarie, A.; Drapeau, G.; Closset, J.; Couture, R.; Adam, A. (1994). «Development of a Digoxigenin-labeled Peptide: Application to a Chemiluminoenzyme Immunoassay of Bradykinin in Inflamed Tissues». Peptides 15 (3): 511-518. PMID 7937327. doi:10.1016/0196-9781(94)90214-3.
- ↑ Mayilo, S.; Ehlers, B.; Wunderlich, M.; Klar, T. A.; Josel, H. P.; Heindl, D.; Nichtl, A.; Kürzinger, K.; Feldmann, J. (2009). «Competitive Homogeneous Digoxigenin Immunoassay Based on Fluorescence Quenching by Gold Nanoparticles». Analytica Chimica Acta 646 (1–2): 119-122. PMID 19523564. doi:10.1016/j.aca.2009.05.023.
- ↑ Goodarzi, M. T.; Rafiq, M.; Turner, G. (1995). «An Improved Multiwell Immunoassay Using Digoxigenin-Labelled Lectins to Study the Glycosylation of Purified Glycoproteins». Biochemical Society Transactions 23 (2): 168S. PMID 7672194.
Enlaces externos
|

