|
Iwanow-ReaktionDie Iwanow-Reaktion, auch Ivanov-Reaktion, ist eine Namensreaktion in der Organischen Chemie und nach dem bulgarischen Chemiker Dimitr Iwanow (1894–1975) benannt. Er beschrieb diese Reaktion erstmals 1931. ÜbersichtsreaktionBei der Iwanow-Reaktion wird über eine Grignard-Verbindung eine Bindung zu einem Elektrophil in α-Position hergestellt. Als Rest (R) können Aryl- und Phenylgruppen fungieren. Des Weiteren werden als Elektrophil (E) hauptsächlich Aldehyde und Ketone eingesetzt.[1]  AllgemeinesDie Reaktion hat je nach Verfahren Ausbeuten von 60 % bis 91 %. Es entstehen dabei zwei Diastereomere, welche chromatographisch an einer stationären Phase von Kieselgel getrennt werden konnten. Dabei wurde herausgefunden, dass ein Diastereomer zu 76 % mit einem Schmelzpunkt von 178 °C und das andere nur zu 24 % mit einem Schmelzpunkt von 143 °C gewonnen werden konnte.[2] ReaktionsmechanismusZunächst wird ein Dianion bzw. das so genannte Iwanow-Reagenz aus Aryl-Essigsäure hergestellt. Dabei findet eine elektrophile Reaktion mit der Grignard-Verbindung statt (1). Hierdurch entsteht eine weitere Carbonylgruppe, welche wiederum auch elektrophil mit einer Grignard-Verbindung reagiert (2). Es entsteht das Iwanow-Reagenz, welches eher einen Ionencharakter von der Bindung her zum Magnesium darbietet (Dianion).  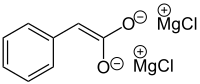 Das Iwanow-Reagenz reagiert mit Elektrophilen, vorzugsweise Carbonylverbindungen (Aldehyde, Ketone), Isocyanaten oder Alkylhalogeniden.[3][4][5][6][7] Im folgenden Beispiel wird das Iwanow-Reagenz aus Phenylessigsäure und zwei Äquivalenten einer Grignard-Verbindung hergestellt. Als Elektrophil wird Benzaldehyd (blau markiert) eingesetzt. In 3 findet ein elektrophiler Angriff des Aldehyds auf die Doppelbindung des Iwanow-Reagenz statt, wobei sich durch Umklappen der Elektronen das Magnesium an den Sauerstoff des Benzaldehyds bindet (4). Durch Hydrolyse wird das Endprodukt 5 erhalten.  StereoselektivitätBei der Iwanow-Reaktion entstehen 2 Diastereomere. Diese entstehen im Verhältnis 76:24. Grund hierfür ist die Sterische Hinderung der Phenylgruppe(n). Diese sterische Hinderung der Iwanow-Reaktion wurde von Zimmermann und Traxler über einen nach ihnen benannten Zimmermann-Traxler-Übergangszustand beschrieben. Toullec et al. haben die Kinetik der Reaktion untersucht.[8][9] Die Stereozentren wurden mit roten Sternchen in der Abbildung markiert.  Siehe auchLiteratur
Einzelnachweise
|